HPGD突变导致罕见的以杵状指趾为主要表现的原发性肥厚性骨关节病家系研究
来源:CSOBMR 发布日期:2018-09-20 15:47:09浏览:4515次
作者:吕芳 宋玉文 李路娇 王鸥 姜艳 夏维波 邢小平 李梅
单位:中国医学科学院 北京协和医学院 北京协和医院内分泌科 国家卫生健康委员会内分泌重点实验室
摘要:目的 调查2例以不明原因杵状指趾为主要表现的儿童患者的临床特点,并对患者及其家系进行致病基因突变研究。方法 纳入2例以杵状指趾为主要表现的女性患儿,详细询问病史,评估患者骨骼影像学特点,测量骨代谢生化指标及骨密度,筛查杵状指趾相关的继发原因,采用Sanger直接测序法检测HPGD基因突变。结果 先证者及其妹妹均在出生6个月后逐渐出现杵状指趾及掌跖多汗,先证者有先天性动脉导管未闭病史。两例患者均无面部皮肤增厚及关节肿胀,X线片未见骨膜增厚等异常表现。2例患者骨吸收指标和骨密度在性别、年龄匹配的正常范围,临床未检出导致杵状指趾的其他疾病。基因检测提示两患者存在HPGD基因第3外显子c.310_311delCT和第3内含子c.324+5G>A的复合杂合突变,其父母亲分别为上述突变的携带者,提示患儿罹患原发性肥厚性骨关节病(primary hypertrophic osteoarthropathy,PHO)。结论 PHO为罕见的遗传性疾病,常呈常染色体隐性遗传,女性患者可能表现不典型,疾病早期可仅有杵状指趾的表现,容易漏诊。检测HPGD等PHO致病基因突变,有助于提高PHO的诊断水平。
关键词:原发性肥厚性骨关节病;杵状指趾;HPGD基因突变
原发性肥厚性骨关节病(primary hypertrophic osteoarthropathy,PHO),又称厚皮性骨病(pachy-dermoperiostosis),为罕见遗传性疾病,多数呈常染色体隐性遗传,主要累及皮肤、骨骼和软组织。疾病的主要临床表现包括杵状指趾、皮肤增厚、骨膜增生、多汗、关节肿痛等,少见表现有动脉导管未闭、颅缝关闭延迟、骨髓纤维化、腹泻等。
近期研究发现,PHO的致病基因主要有:编码15-羟前列腺素脱氢酶(15-hydroxyprostaglandin dehydrogenase,15-PGDH)的HPGD基因和编码前列腺素转运蛋白(prostaglandin transporter,PGT)的SLCO2A1基因。目前国内外报道的患者多为男性,大多具有皮肤增厚、骨膜增生、关节肿胀等典型临床表现,然而,PHO女性患者少,临床表现相对不典型,容易漏诊,报道较少。
据文献报道,杵状指趾是PHO最常见的临床表现之一。约95%~97%的杵状指趾存在复杂的继发性原因,主要与心、肺疾病,消化系统疾病和肿瘤等疾病相关。明确杵状指趾的原因相对困难,疾病的治疗也面临挑战,积极寻找其病因对于进一步治疗,具有重要意义。
本研究对两例罕见的主要表现为原因不明杵状指趾的女童,进行临床表型的详细调查,并对其致病基因突变进行检测,旨在了解导致患者杵状指趾的可能机制。
对象与方法
对象
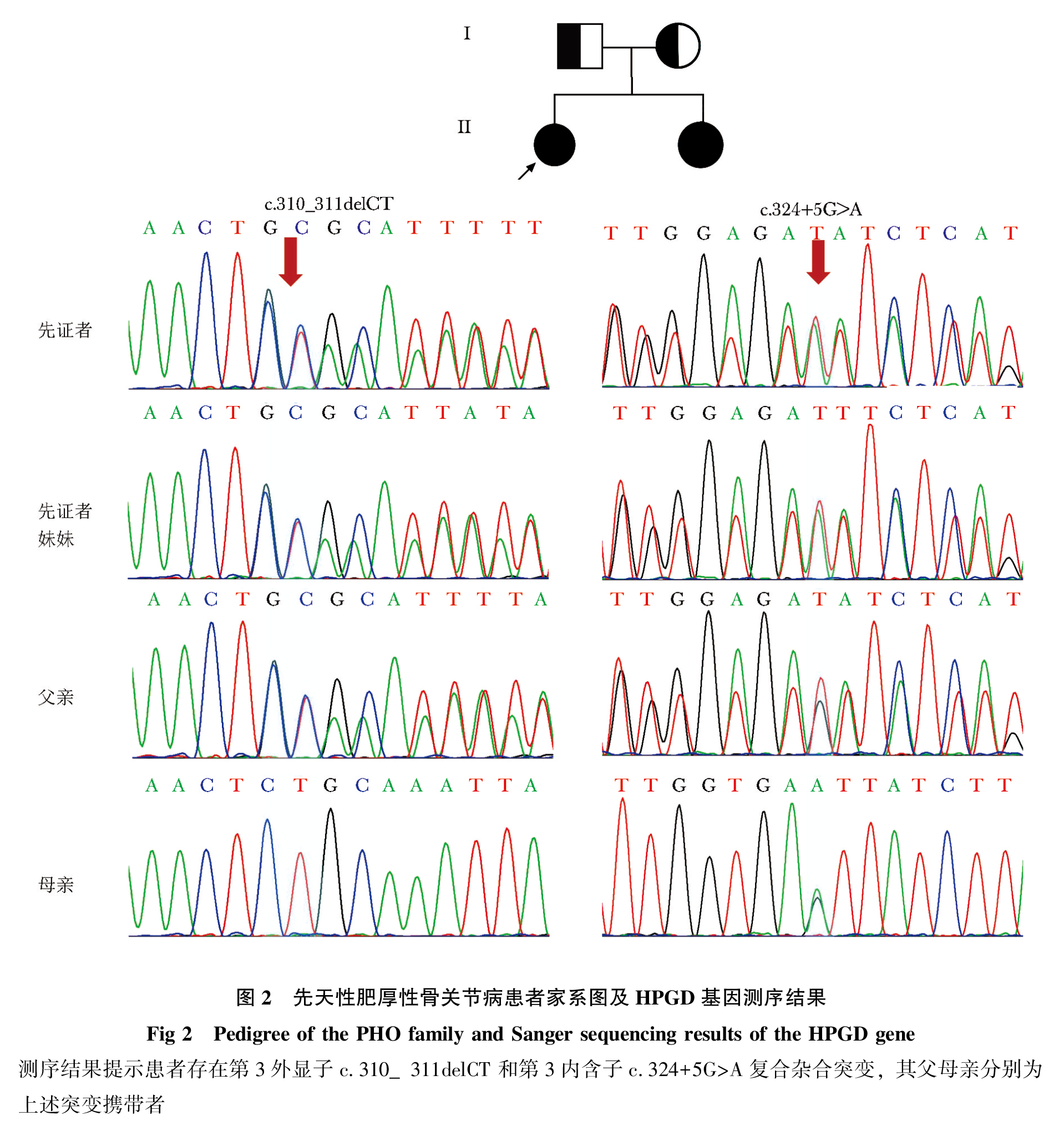
先证者,女,年龄9岁3个月,主诉:发现杵状指趾8年余。先证者妹妹,年龄4岁8个月,主诉:发现杵状指趾4年余。2例患者于2017年8月就诊于北京协和医院内分泌科。患者母亲孕期平顺,2例患者均足月剖腹产,出生体质量3.0 kg左右,身长不详。患者均于6月龄出现杵状指趾,并逐渐出现掌跖多汗。否认关节肿痛、面容变丑、皮肤增厚、腹泻、胃部不适、贫血病史。既往:姐姐罹患先天性动脉导管未闭,手术治疗后好转。妹妹曾右侧锁骨骨折。家族史:父母亲非近亲婚配,体健,否认家族中类似病史。查体:先证者身高145 cm(位于同龄同性别儿童+1 SD~+2 SD),体质量45 kg(位于同龄同性别儿童+2 SD ~+3 SD)。可见典型杵状指趾,掌跖多汗,掌部皮肤粗糙。妹妹:身高115 cm(位于同龄同性别儿童+1 SD~+2 SD),体质量19.5 kg(位于同龄同性别儿童中位数~+1 SD),可见典型杵状指趾,掌跖多汗(图 1)。两患儿均无面部皮肤增厚,无关节肿痛,无骨骼畸形,无紫绀,囟门已闭。患者家系图如图2所示。
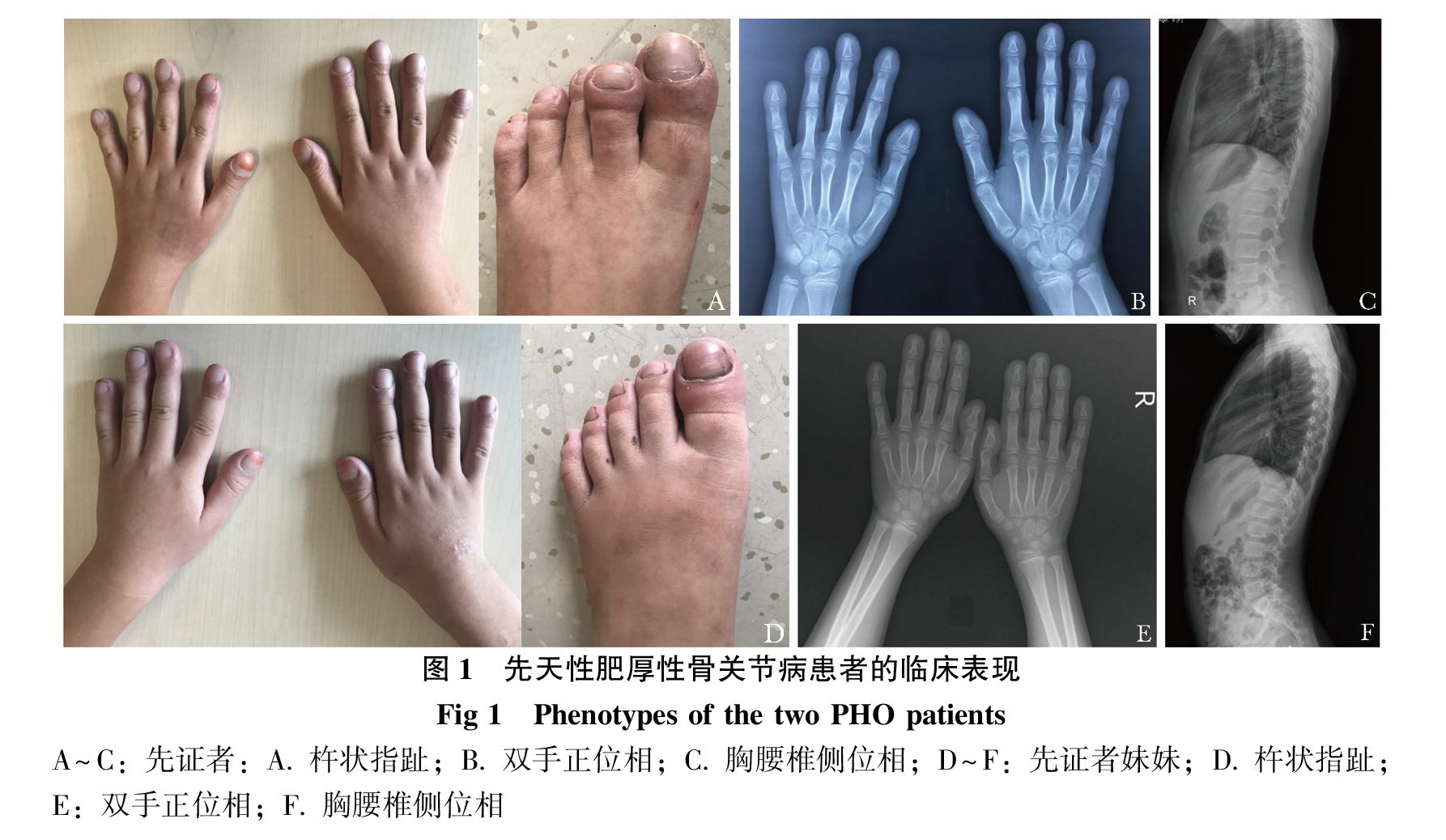
先证者及妹妹血生化指标和骨密度(bone mineral density,BMD)检测结果见表 1。血气分析结果正常,无低氧血症。患者血清钙、磷、甲状旁腺素浓度在正常范围,骨形成指标碱性磷酸酶正常,骨吸收指标β-胶原降解产物符合儿童正常范围,血清25OHD水平正常。患者骨密度在同龄儿童的正常范围。X线片未见掌骨及尺桡骨骨膜增生及肢端骨溶解表现,胸腰椎无侧突、后突畸形及压缩性骨折(图 1)。
本研究获北京协和医院科研伦理委员会批准,在研究开始前征得患者父母同意并签署知情同意书。

致病基因检测
采集先证者、妹妹及其父母外周静脉血,提取基因组DNA(采用德国QIAampDNA Blood mini试剂盒)采用Primer3软件设计引物,扩增HPGD的1~7外显子及其与内含子交界区。引物序列、扩增长度及PCR反应条件见表2。PCR扩扩增产物纯化后用荧光自动测序仪(ABI3700,美国)直接测序,测序结果与参考序列NM_000860.5比对,以确定HPGD突变位点及类型,并进一步与NCBI SNP、人类基因突变数据库(http://www.hgmd.cf.ac.uk/ac/index.php)进行比对,排除变异位点为基因多态性位点,并确定其是否为未报道过的新突变位点。采用BioEdit(7.0.9.1)软件分析突变位点在不同物种中的保守性,采用NNSPLICE0.9(http://www.fruitfly.org/)和NetGene2 Server(http://www.cbs.dtu.dk/services/NetGene2/)软件对剪切位点突变进行致病性预测。

结果
患者临床特点
2例患者均为婴儿期起病,主要表现为典型杵状指趾、掌跖多汗,先证者有先天性动脉导管未闭病史,两例患者均未发现心肺系统疾病、Graves病、炎症性肠病等继发性杵状指趾原因。2例患者无面部皮肤增厚、容貌变丑及关节肿痛等表现,影像学未见骨膜增生及肢端骨溶解的异常表现。
HPGD基因突变分析
候选基因PCR产物Sanger测序结果提示患者存在HPGD基因第3外显子c.310_311delCT和第3内含子c.324+5G>A的复合杂合突变(图 2)。患者父亲与母亲分别为c.310_311delCT及c.324+5G>A携带者(图 2)。
讨论
本研究采用分子诊断的方法确诊两例以杵状指趾、掌跖多汗为主要表现的PHO女性儿童患者。患者PHO表现不典型,无明显皮肤增厚、骨膜增生及关节肿痛等表现。基因检测提示患者存在HPGD基因第3外显子c.310_311delCT和第3内含子c.324+5G>A的复合杂合突变。
PHO为罕见遗传性疾病,最早于1868年由德国Friedreic报道,以常染色体隐性和不完全外显的常染色体显性两种方式遗传,男女比例约为4.9:1,2008年和2012年研究发现HPGD和SLCO2A1为该病致病基因。上述基因突变分别影响前列腺素E2(prostaglandin E2,PGE2)的代谢和转运,导致常染色体隐性遗传1型PHO(PHOAR1,OMIM 259100)和常染色体隐性遗传2型PHO(PHOAR2,OMIM 614441)。HPGD基因位于HPGD基因位于4q34.1,共有7个外显子,编码266个氨基酸的15-羟前列腺素脱氢酶,主要负责在细胞内将PGE2降解为PGE-M。SLCO2A1位于3q22.1-q22.2,编码643个氨基酸的前列腺素转运蛋白,主要介导PGE2从细胞外进入细胞内。HPGD和SLCO2A1突变均导致体内PGE2增多,PGE2可以扩张血管,促进局部组织增生,刺激成骨细胞和破骨细胞,从而导致杵状指趾、多汗、骨膜增生、肢端骨溶解等临床表现。在胎儿期,动脉导管在胎盘产生的PGE2作用下保持开放,出生后血PGE2浓度明显降低,动脉导管关闭,但是,由于PHO患者血液PGE2浓度不能迅速下降,可能导致动脉导管无法关闭,本例先证者就存在动脉导管未闭而行手术治疗,这也是疾病表型的一部分。
PHOAR1和PHOAR2两种疾病亚型可以通过起病年龄、性别分布和并发症进行临床鉴别。HPGD突变患者通常起病年龄早,男女比例约为2:1。SLCO2A1突变患者起病年龄较晚,多于青春期后起病,尚无关于女性患者的报道。有研究者提出性激素水平可能对PGT有影响,可以解释起病年龄和性别分布的差异,但在大样本PHO患者中,未发现尿PGE2和PGE-M与性激素水平有相关性,因此,PHOAR1和PHOAR2患者起病年龄和性别分布存在差异的机制,有待深入研究。PHOAR1型和PHOAR2型临床表型和并发症也存在差异。PHOAR2型患者通常皮肤增厚较PHOAR1型明显,可能与PHOAR2型患者的PGE2水平更高相关。PHOAR2型患者容易并发骨髓纤维化和胃肠道出血,提示PGT对造血干细胞的诱导和维持,以及黏膜稳态具有重要作用。尚未见PHOAR2型患者有动脉导管未闭的报道,可能是由于SLCO2A1突变患者出生后存在其他方式降解PGE2,使动脉导管关闭,但其机制尚需进一步探索。由于本研究两例患者均为女性,出生后6个月即起病,先证者又有动脉导管未闭病史,临床推测患者可能为PHOAR1型,经致病基因突变检测,证实患者存在HPGD基因的复合杂合突变,确认患者为PHOAR1型。
随着分子遗传学的研究进展,越来越多的PHO患者获得分子诊断。研究总结的41例PHO患者全部为男性,研究总结的27例PHO患者中,仅1例为女性,提示该病男性多见,但也可能女性患者临床表现较轻,容易漏诊。但也有1例北京协和医院女性PHO患者出现杵状指、掌跖多汗、手掌皮肤增厚、骨膜增生和关节疼痛等典型PHO临床表现的报道。本研究报道的两例患者均为女性,临床表现较轻,仅以杵状指趾及掌跖多汗为主要临床表现,1例患者有动脉导管未闭史,患者无面部皮肤增厚、骨膜增生和关节肿痛的表现,这与文献报道的女性患者的临床表现相似。本研究患者就诊年龄较小,也可能疾病表现较轻与病程短有关,未来尚需对患者进行长期随访。
在鉴别诊断方面,杵状指趾尚需考虑其他疾病所致的可能,包括心、肺疾病,血管性病变,炎症性肠病,Graves病等。本研究2例患者无上述疾病的临床表现,经过相应检查,也未见上述疾病的诊断证据。本研究先证者有动脉导管未闭病史,这可见于多种遗传性疾病,如Rubinstein-Taybi综合征、Char综合征等,上述综合征多有典型外貌畸形,通过致病基因突变检测,能够很好地进行鉴别诊断。本研究提示,对于典型杵状指趾的患者,仍需考虑PHO的可能,进行致病基因突变检测,对于明确病因十分必要。
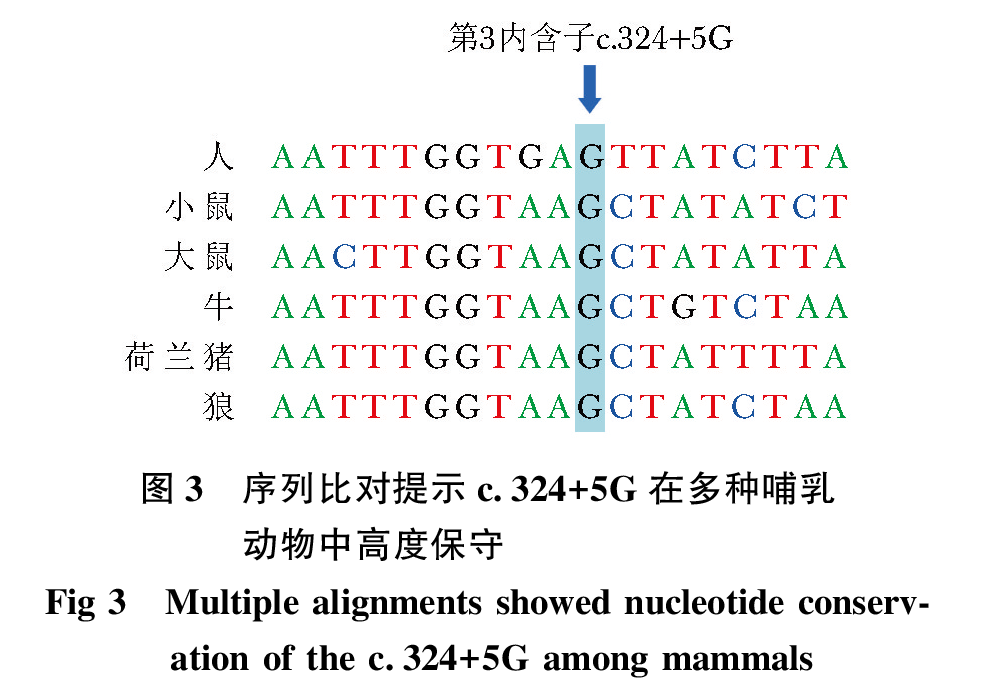
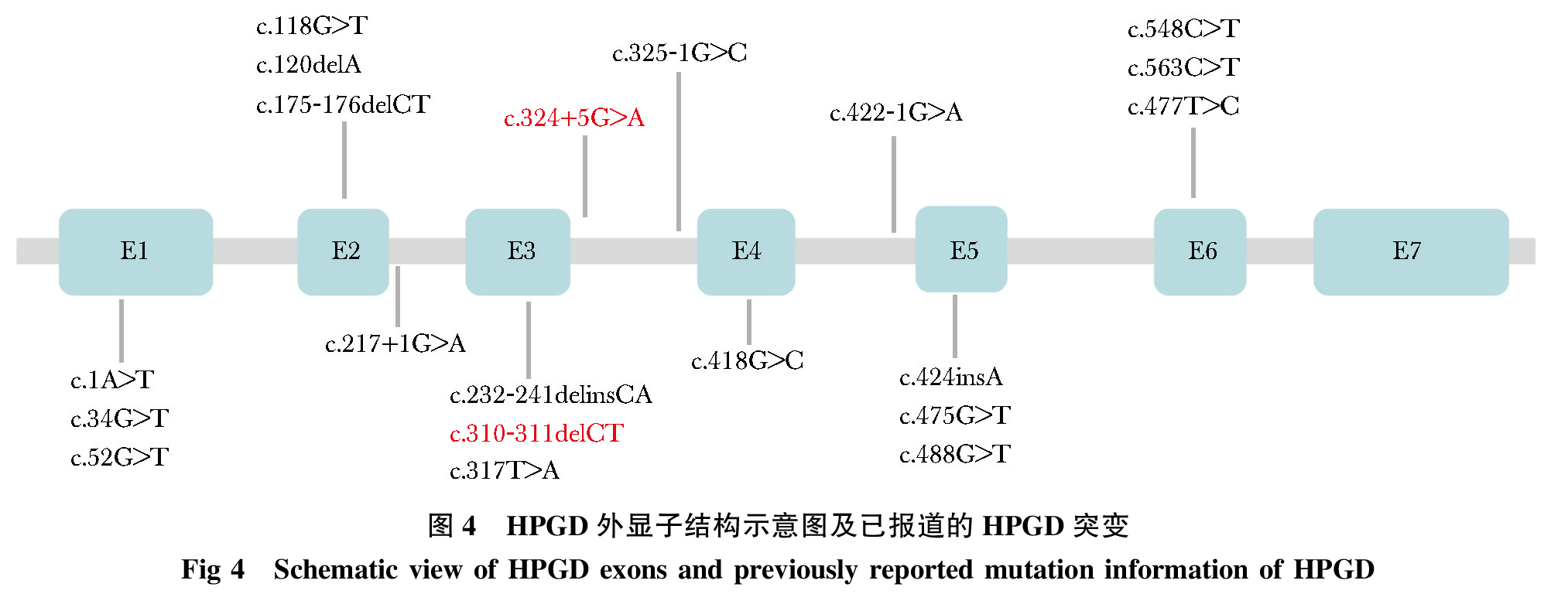
目前已报到的HPGD突变至少有20种(图 3,4),分布在第1~6外显子、第2~4内含子区域,其中c.175_176delCT突变(p.L59VfsX8)为欧洲患者的热点突变。本研究发现患者存在HPGD复合杂合突变,其中c.310_311delCT突变由Erken等首次报道,此突变在中国人群中被多次报道,为中国人群HPGD突变患者的热点突变位点,其可致104位后氨基酸框移突变,并产生截短蛋白(p.L104AfsX3)。本研究检出的另一种突变c.324+5G在人、小鼠、大鼠、牛、荷兰猪、狼等多个物种中高度保守(图 3),在中国人群中也已被报道,软件预测该突变可导致剪切位点突变,引起外显子跳跃,使得蛋白质结构改变。
在治疗方面,由于杵状指趾通常无症状,往往不需要治疗。有关节肿痛或皮肤增厚的患者,可给予非甾体抗炎药治疗,针对PEG2的选择性环氧化酶-2抑制剂为首选,该药可抑制花生四烯酸转化为前列腺素环内过氧化物,降低PEG2水平,改善患者症状。我国大样本研究前瞻性观察41例PHO患者,给予依托考昔60 mg/d治疗6个月,发现患者皮肤增厚、杵状指趾、关节肿痛明显改善,但骨皮质增厚变化不明显,该药能否改善骨骼异常尚需长期观察。另外,有研究报道对非甾体类抗炎药抵抗的患者,试用双膦酸盐或英夫利西单抗治疗,对部分患者有效。本项研究2例患者仅有杵状指趾表现,目前无临床症状,暂未予治疗,随访观察中。
PHO为罕见遗传性疾病,女性患者尤为罕见,且临床表现不典型。本文报道2例女性PHO患儿,仅以杵状指趾和掌跖多汗为临床表现,无面部皮肤增厚、骨膜增生、关节肿痛和肢端骨溶解等表现,基因检测证实HPGD复合杂合突变为患者的致病原因。提示对于起病较早的以杵状指趾为主要表现的患者,需重视HPGD等基因突变检测,以排查PHO的可能性。